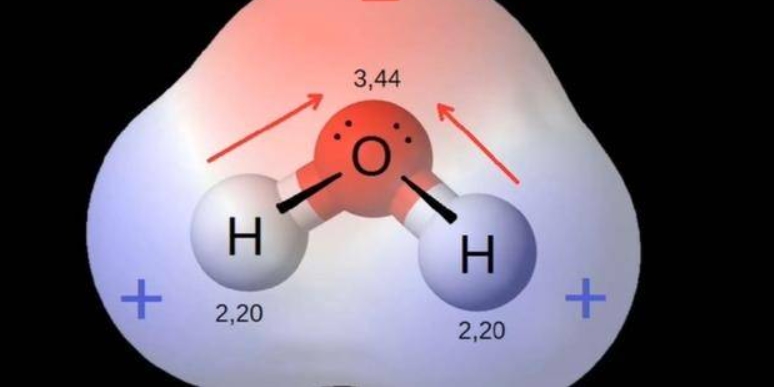
分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,这样的分子为极性分子。一般从结构和溶解性上可以做出判断:有暴露的羟基,暴露的羧基,暴露的氨基的物质极性可能很大;然后溶解性实验,溶剂的极性一般与物质极性一致。
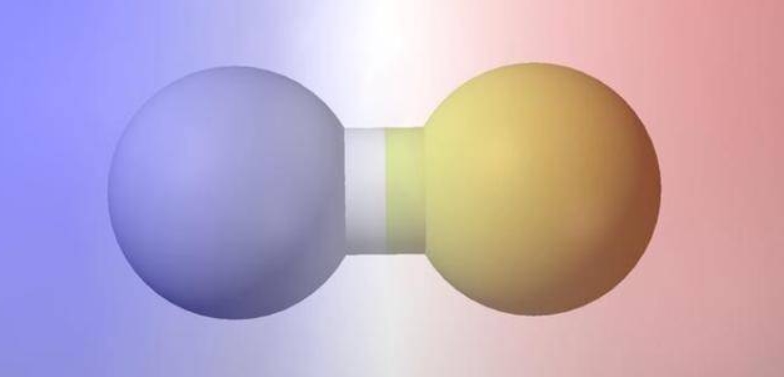
极性分子是指正负电荷中心不重合的分子,以极性键结合的双原子分子一定为极性分子,极性键结合的多原子分子视结构情况而定如CH4就不是极性分子,组成为ABn型化合物,若中心原子A的化合价等于族的序数,则该化合物为非极性分子。
分子极性是什么
分子极性即分子中正负电荷中心不重合,导致电荷的分布不均匀所产生的极性,共价键的极性是因为成键的两个原子电负性不相同而产生的,电负性高的原子会把共享电子对“拉”向它那一方,使得电荷不均匀分布,键的极性程度可以用两个原子电负性之差来衡量,差值在0.4到1.9之间的是典型的极性共价键。
极性是什么
物体在相反部位或方向表现出相反的固有性质或力量,对特定事物的方向或吸引力,如果电荷分布得不均匀,则称该键或分子为极性;如果均匀,则称为非极性,物质的一些物理性质(如溶解性、熔沸点等)与分子的极性相关,而对两极或起电(如物体的)特定正负状态。